Anvisa concede registro definitivo para a vacina da Pfizer
Segundo a Anvisa, entre as autoridades referendadas pela Organização Pan-Americana da Saúde (Opas), a agência reguladora brasileira é a primeira a conceder o registro de uma vacina contra a Covid-19.
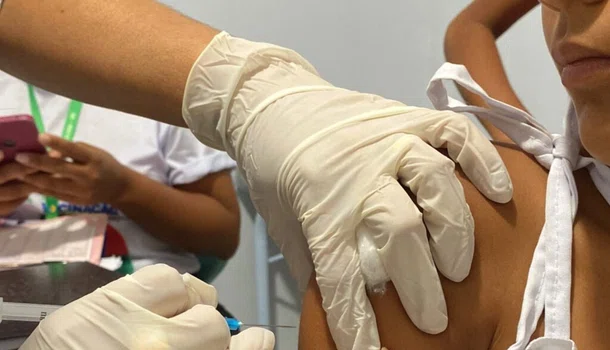
Na manhã desta terça-feira (23), a Agência Nacional de Vigilância Sanitária (Anvisa) concedeu o registro definitivo à vacina contra a Covid-19 desenvolvida pela farmacêutica norte-americana Pfizer em parceria com a empresa de biotecnologia alemã BioNtech.
A concessão do registro foi anunciada pelo diretor-presidente da agência reguladora, Antônio Barra Torres, que destacou que a análise para a liberação do imunizante levou 17 dias.
A empresa entrou no dia 6 de fevereiro com o pedido de registro definitivo da vacina contra a covid-19. O imunizante Cominarty entretanto, ainda não está disponível no país. A vacina é a primeira a obter o registro definitivo no Brasil.
Em dezembro, a Pfizer já havia anunciado que não faria pedido para uso emergencial da sua vacina no Brasil, e que seguiria o processo de submissão diretamente para um registro definitivo. À época, a empresa disse considerar o procedimento “mais célere”, além de mais amplo. Segundo a Pfizer, 2,9 mil voluntários participaram dos testes clínicos de sua vacina no Brasil.
No mundo todo, foram 44 mil participantes em 150 centros de seis países, incluindo África do Sul, Alemanha, Argentina, Estados Unidos e Turquia. Os resultados da terceira e última fase de testes do imunizante, divulgados em novembro, apontaram eficácia de 95% contra o novo coronavírus (covid-19). De acordo com a Anvisa, o registro “abre caminho para a introdução no mercado de uma vacina com todas as salvaguardas, controles e obrigações resultantes dessa concessão”.
Até o momento, as vacinas aprovadas no Brasil são para uso emergencial: a CoronaVac, produzida pelo Instituto Butantan em parceria com a farmacêutica chinesa Sinovac, e a vacina produzida pela Fundação Oswaldo Cruz (Fiocruz) em parceria com a Universidade de Oxford e o laboratório inglês AstraZeneca.
Segundo a Anvisa, entre as autoridades referendadas pela Organização Pan-Americana da Saúde (Opas), a agência reguladora brasileira é a primeira a conceder o registro de uma vacina contra a Covid-19.
O pedido de registro definitivo é o segundo que a Anvisa recebe para uma vacina contra a covid-19. O primeiro foi feito em 29 de janeiro e é relativo à vacina desenvolvida pela farmacêutica AstraZeneca em parceria com a Universidade de Oxford, que já tem autorização para uso emergencial no país.
Com informações da Agência Brasil.
Saiba como fazer a prevenção de cinomose canina nos pets
O imunizante, Vanguard Plus, utilizada contra a cinomose e outras doenças está disponível na Clínica-Escola da UNINASSAU Jockey.Esperantina alerta para vacinação contra a gripe de pessoas com doenças crônicas
As autoridades de saúde reforçam o apelo sob o lema de que "A vacinação salva vidas!", incentivando os cidadãos a garantirem sua dose para a proteção individual e coletiva de toda a comunidade.Hospital Regional Tibério Nunes contará com mais de 300 leitos após obras em Floriano
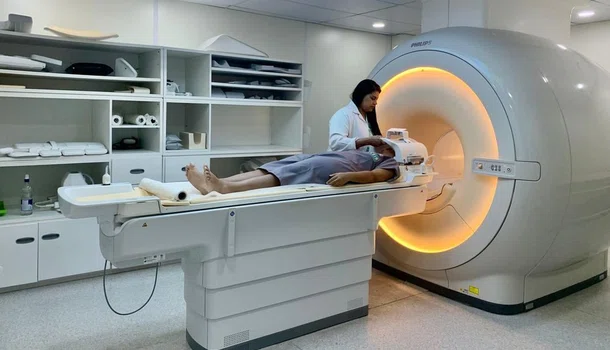
Conforme a Sesapi, os investimentos em estrutura e ampliação dos serviços ultrapassam R$ 18 milhões.Mais de 20 municípios do Piauí são beneficiados com Carreta de Ressonância Magnética
De acordo com a Secretaria de Estado da Saúde do Piauí (Sesapi), o projeto do Ministério da Saúde garante acesso a exames especializados.FMS amplia vacinação contra gripe para novos grupos prioritários em Teresina
A FMS ressalta que, a vacina está disponível de segunda a sexta-feira, nos turnos manhã e tarde, em todas as 91 UBS de Teresina.







E-mail
Messenger
Linkedin
Gmail
Tumblr
Imprimir